2021年度睡眠医学十大科学进展
本文来源:神经科学论坛
01
Nat Commun:沉睡时,我们大脑在想些什么?
人类有三分之一的时间在睡眠中度过。但是,大脑在这么长的时间里做了些什么呢?由于人类还没有找到可以翻译大脑活动的工具,因此,我们目前仍然无法知道大脑在睡眠中到底想了些什么。然而,我们知道睡眠对巩固记忆和情绪管理起着重要作用:当我们睡着后,我们的大脑就会重新激活白天建立的记忆轨迹,帮助我们调节情绪。

研究在比较了清醒时和睡眠阶段的MRI扫描结果发现,大脑在深度睡眠期间的激活模式与游戏阶段记录活动方式的非常相似。而且,很明显,大脑通过激活清醒时使用的区域,重新体验了游戏的胜利,而不是游戏的失败。你一入睡,大脑活动就会改变。随着睡眠的深入,志愿者的大脑又开始“思考”这两个游戏,而且,有意思的是,大脑在进入深度睡眠时几乎只考虑自己获胜的游戏。
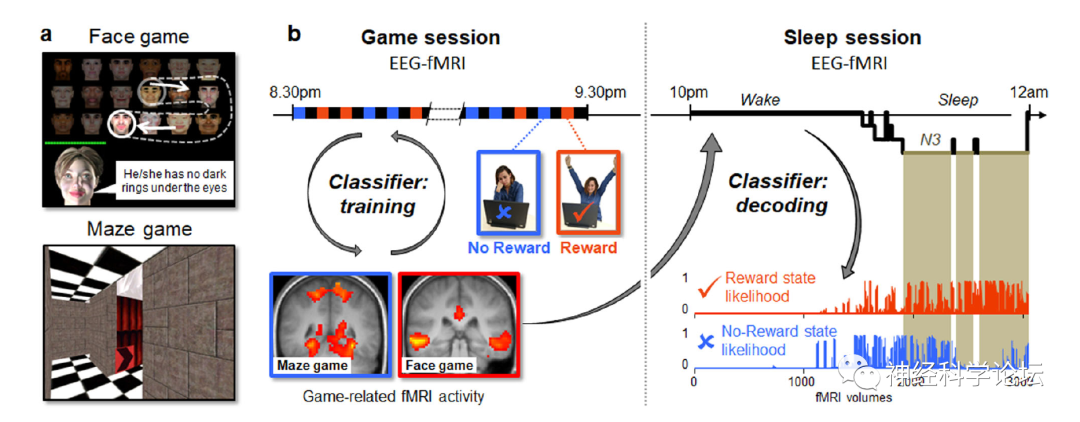
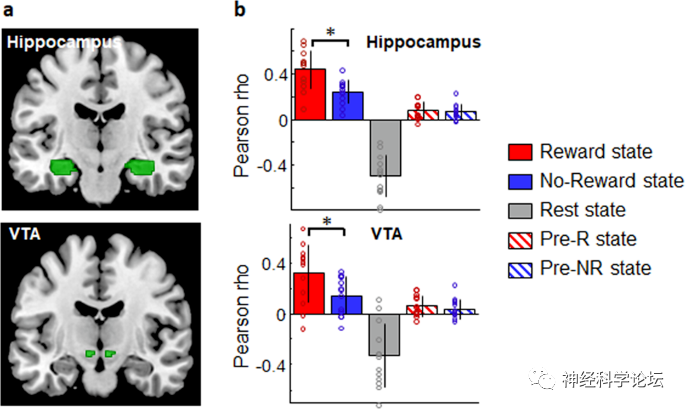
两天后志愿者们进行了一项记忆测试:一个是识别游戏中的所有面孔,另一个是找到迷宫的起点。同样,和游戏有关的脑区在睡眠中激活的越多,记忆表现就越好。也就是说,当奖赏在睡眠中被自发激活时,与奖赏又关的记忆会更强。这项研究拓展了睡眠中大脑的研究方法,在大脑每天晚上睡眠中所做的不可思议的工作方面开辟了一个新的视角。
信源:Sterpenich V, et al. Reward biases spontaneous neural reactivation during sleep. Nat Commun. 2021 Jul 6;12(1):4162. doi: 10.1038/s41467-021-24357-5.
02
Science子刊:睡得越少会导致“傻”得越快!
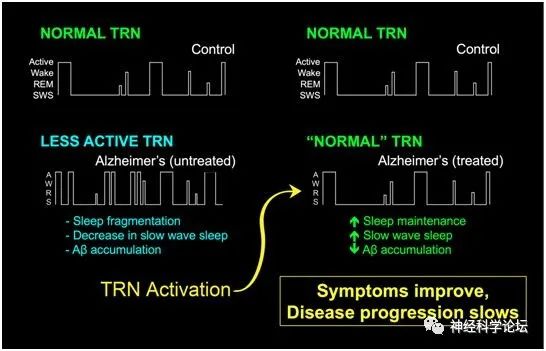
研究再通过使用化学遗传系统(一种允许人们以化学方式激活特定细胞的技术)激活AD小鼠模型中的TRN神经元。研究发现在对TRN进行单轮化学遗传激活后,AD小鼠醒来的次数减少,慢波睡眠的时间增加,睡眠的持续改善以及Aβ的积累显著减少。
信源:Rohan Jagirdar, et al. Restoring activity in the thalamic reticular nucleus improves sleep architecture and reduces Aβ accumulation in mice. Science Translational Medicine, 2021, doi:10.1126/scitranslmed.abh4284.
03
Brain:为何一天睡10个小时还是精神不振?

为了验证这一假设,研究人员在100名参与者中监测了4-6个晚上的睡眠-觉醒活动,这些参与者纵向接受了标准化的认知测试、APOE基因分型以及AD生物标志物、CSF中总tau和Aβ42的测量。
为了评估认知功能,患者在每次临床就诊时都要完成神经心理学测试,包括自由和提示选择性记忆测试、逻辑记忆延迟回忆评估、数字符号替代测试和迷你精神状态检查。在队列中对这四项测试中的每一项进行Z型评分,并取其平均值来计算临床前AD的认知综合得分。使用广义加性混合效应模型估计了横断面睡眠参数对纵向认知表现的影响。
结果显示睡眠时间单独就足以影响大脑认知能力的变化——在7-8小时睡眠时长时认知受损风险最低。由认知综合指标衡量的认知功能的纵向变化在总睡眠时间(P<0.001)、非快速眼动睡眠时间(P<0.001)和快速眼动睡眠时间(P<0.001)、睡眠效率(P<0.01)以及<1 Hz和1-4.5 Hz非快速眼动慢波活动(P<0.001)低值和高值时都有所下降。
在总睡眠时间、非快速眼动睡眠和快速眼动睡眠时间以及<1Hz慢波活动的中间范围内,认知功能随着时间的推移而稳定,这表明某些水平的睡眠对维持认知功能很重要。提高睡眠效率而非睡眠时长才是预防认知功能下降最关键的因素。
信源:Lucey BP, et al. Sleep and longitudinal cognitive performance in preclinical and early symptomatic Alzheimer's disease. Brain. 2021 Oct 20;144(9):2852–62. doi: 10.1093/brain/awab272.
04
Nat Commun:揭示Nf1基因调节睡眠-觉醒周期机制

研究利用检测管子里的果蝇运动的红外传感器分析它们的睡眠-觉醒周期。在24小时内,果蝇在晚上睡觉约10小时,然后整个白天活动,除了约4至5小时的午睡。对那些睡眠-觉醒周期失调的大脑特定区域(因其特有的形状而被称为“蕈形体”)受到损害的果蝇,并分析了健康果蝇大脑中这个区域的基因表达。
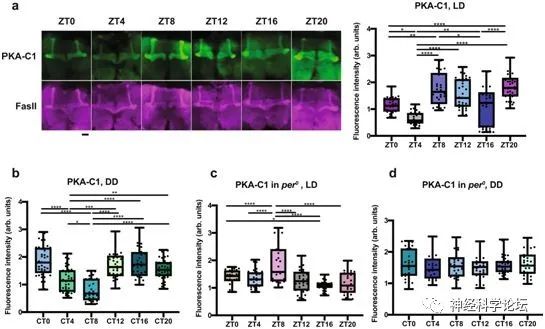
研究发现一个称为Nf1的基因的表达根据果蝇的睡眠-觉醒周期而波动。当果蝇醒着的时候,它的表达增加了,而在它们的睡眠期间,它的表达减少了。为了证实这个基因和昼夜节律之间的联系,这些作者观察了那些不管一天中的什么时候微弱地表达这个基因的果蝇。这些果蝇完全失调,而且有更多的睡眠周期。
NF1蛋白位于触发钙释放的调节级联的上游,而钙是激活大脑蕈形体中的神经元所必需的。Nf1的表达导致大脑这一区域的神经元在白天比晚上更活跃,从而促进了白天的清醒。Nf1的人类同源物是一个防止神经系统中肿瘤产生的基因。
信源:Pedro Machado Almeida, et al. Neurofibromin 1 in mushroom body neurons mediates circadian wake drive through activating cAMP–PKA signaling. Nature Communications, 2021, doi:10.1038/s41467-021-26031-2.
05
Sleep:轮班工作者的睡眠与其睡眠类型有关联
轮班工作是我们24/7(一天24小时,一星期7天)社会的一个重要组成部分,其会不可避免地导致人体习惯性睡眠时间的转移,从而引发机体内部昼夜节律系统与休息-活动周期和环境的不一致或不协调;目前研究人员并不清楚在轮班工作中个体间的中也节律组织差异是如何影响机体的睡眠时间和持续时间的。获得足够的睡眠对于轮班/夜班工人而言是一项真正的挑战,其会影响机体的整体健康,那么作为早起的鸟儿或夜猫子在机体获得良好的睡眠方面扮演着什么样的作用呢?
一项来自麦吉尔大学等机构的研究发现,睡眠类型(chronotype)和轮班工人从不规则的时间表中可以获得的睡眠量之间或许存在一定关联。研究成果发表在2021年2月Sleep杂志上。
有些人天生喜欢早睡,而其他人则更倾向于晚睡;这种偏好被称为睡眠类型,其是由机体中的昼夜节律系统(每个人机体独特的内部计时器)来调节。研究人员通过研究首次分析了早班、晚班和夜班工人的睡眠类型和其睡眠行为之间的关联;在将近一个月的时间里,这些工人都佩戴者类似手表的装置来测定其睡眠状态。
并非所有的轮班都是平等的,研究发现睡眠类型对于睡眠持续时间和午睡行为的影响取决于轮班的类型,平均而言,早起的人会在早班时能多睡1.1个小时,而夜猫子在晚班时则能多睡2个小时。虽然轮班工人会通过小睡来减少不规则睡眠时间表对其睡眠的影响,但这种行为在早起者上夜班时表现尤为明显;一般而言,与夜猫子相比,早起者在上完夜班后睡得更少,但他们在上夜班之前会有更多的小睡,因此他们每天总的睡眠时间是相似的。
研究发现或能帮助研究人员设计出新型策略来改善非典型时间表的工人的睡眠,而诸如此类策略则可以包括考虑睡眠类型原理的工作安排等。参与轮班工作的人群都会经历睡眠障碍和支离破碎睡眠时间风险的增加;由于睡眠对于机体的最佳表现、健康和幸福至关重要,希望能够设计出新型策略来让这些轮班工作者获得更好的睡眠。
信源:Kervezee L, et al. The relationship between chronotype and sleep behavior during rotating shift work: a field study. Sleep. 2021 Apr 9;44(4):zsaa225. doi: 10.1093/sleep/zsaa225.
06
npj Digital Medicine:揭示睡眠影响情绪的机制
睡眠具有一个多维度的结构,睡眠的质量、持续时间、连续性、昼夜节奏、规律性等度量指标都是评价睡眠健康的参数。“晚上不睡,白天崩溃” 并非危言耸听,生活经验告诉我们,睡眠质量的好坏直接影响了第二天的精神状态和身体健康。
一项来自美国密歇根大学学术医学中心新研究中通过对2100多名职业早期的医生一年内的睡眠和情绪的直接测量数据进行分析表明,不规律的睡眠与整体睡眠时间不足或经常熬夜一样,会增加个体长期抑郁的风险。相关研究结果发表在2021年2月的npj Digital Medicine期刊上。

信源:Fang, Y., et al. Day-to-day variability in sleep parameters and depression risk: a prospective cohort study of training physicians. NPJ Digit Med. 2021 Feb 18;4(1):28. doi: 10.1038/s41746-021-00400-z.
07
Sci Adv:深度睡眠可有效清除大脑垃圾

研究表明,深度睡眠有利于废物清除,并有助于损伤的恢复。清除废物通常对保持大脑健康或预防神经再生性疾病很重要,尽管清醒和睡眠期间可能都会进行废物清除,但深度睡眠期间的废物清除活动会显著增强,这种被清除的废物包括可能导致许多神经退行性疾病的有毒蛋白质。
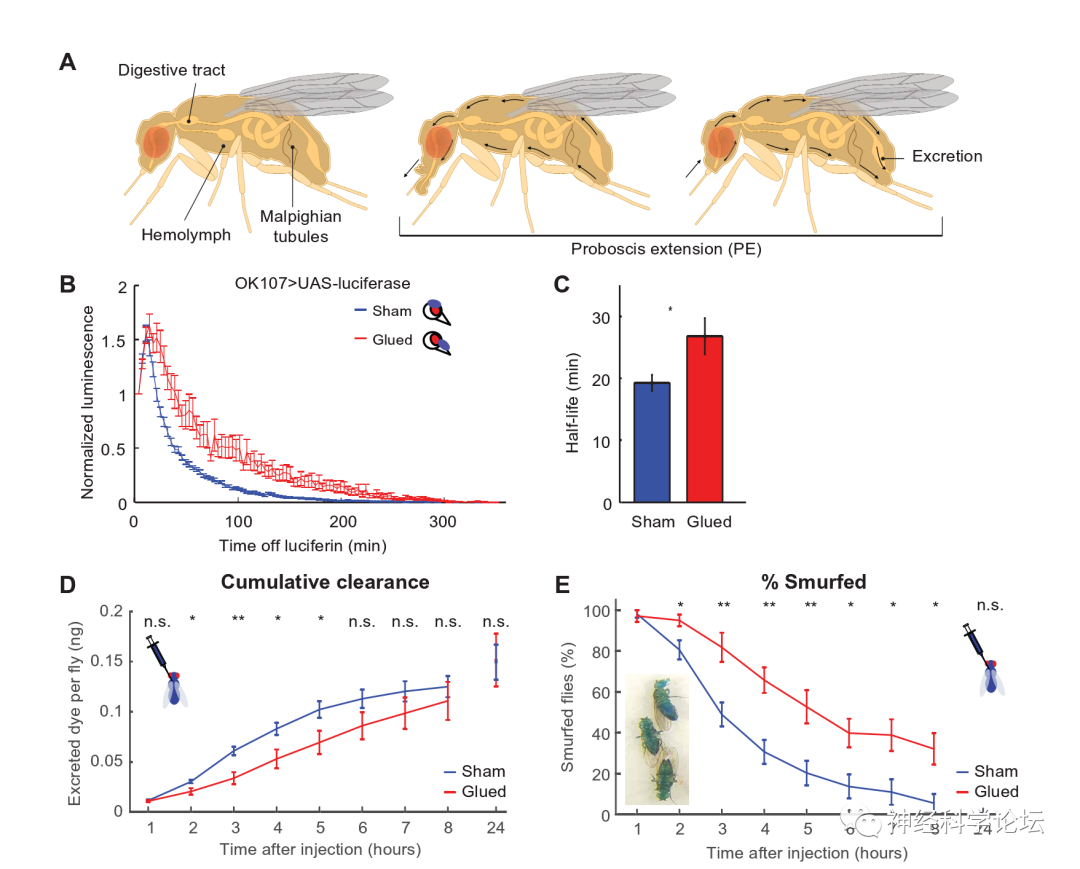
这项研究使我们更加了解为什么所有生物都需要睡眠的奥秘。所有动物,尤其是野外的动物,入睡时都极度脆弱。但是越来越多的研究表明,睡眠的好处(包括重要的废物清除)远远超过了这种增加的脆弱性。深睡眠在果蝇的废物清除中起作用,这表明废物清除是睡眠的进化保守的核心功能,废物清除可能是苍蝇和人类共同祖先的睡眠功能。
信源:van Alphen B, et al. A deep sleep stage in Drosophila with a functional role in waste clearance. Sci Adv. 2021 Jan 20;7(4):eabc2999. doi: 10.1126/sciadv.abc2999.
08
晚上10点到11点睡觉对心脏最健康

该研究包括2006年至2010年期间招募的88026名参与者,他们年龄在43岁至79岁之间,平均年龄为61岁,女性占58%。研究团队通过让参与者佩戴腕戴式加速度计收集他们7天内入睡和醒来的时间,并对参与者进行了生活方式、健康状况、身体评估等调查。然后他们接受了心脑血管疾病的诊断。
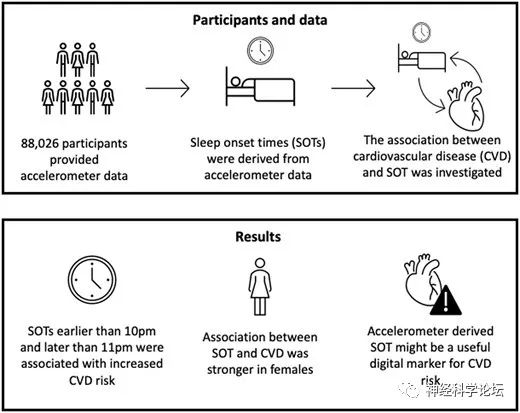
在之后平均为5.7年的随访期间,有3172名参与者(3.6%)患上了心血管疾病。其中,睡眠时间在午夜或更晚的参与者的心血管疾病发病率最高,而在晚上10点至11点入睡的人心血管疾病发病率最低。进一步性别分析显示,女性的入睡时间与心血管风险增加的相关性更强。
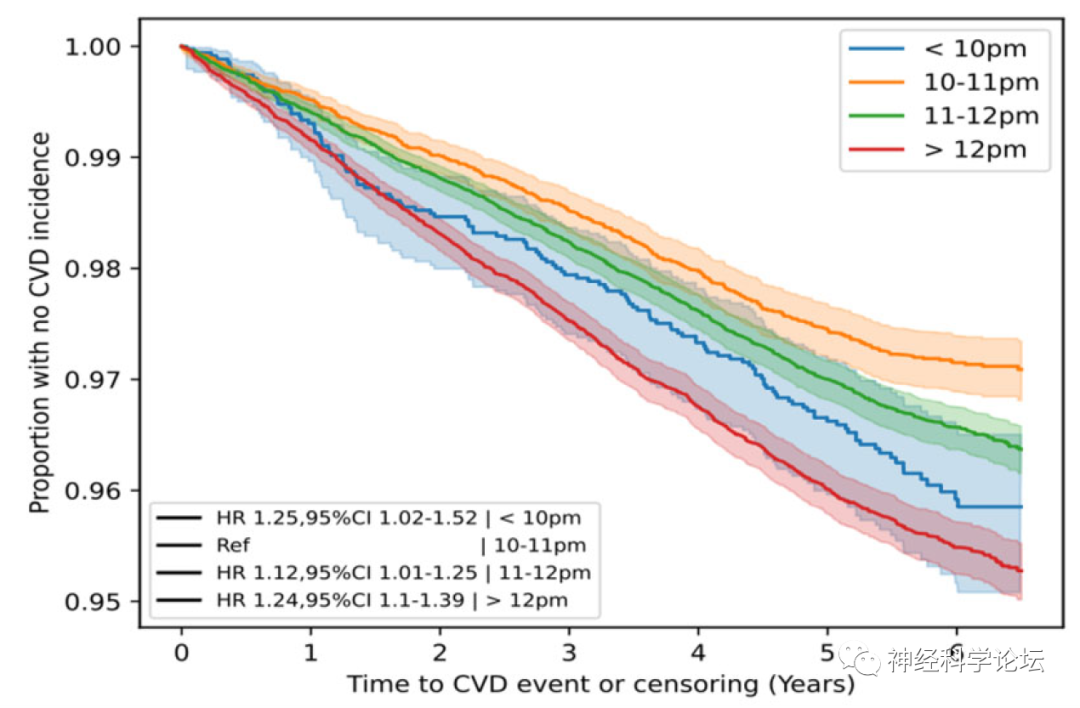
研究显示与晚上10点至11点入睡相比,在晚上12点或之后入睡的人患心血管疾病的风险高出25%,在晚上11点到12点之间入睡的风险高出12%,而在晚上10点之前入睡的人患心血管疾病的风险高出24%。这项研究表明,人们最佳入睡时间点是相对固定的,如果产生偏差可能对健康有害,危害性最大的是在午夜12点之后入睡,这可能是因为睡得太晚,要么第二天起得太晚,减少了看到晨光的可能性,要么第二天正常起床,导致睡眠时间不够,这都会影响到生物钟。虽然这些研究结果没有显示出因果关系,但仍然能看出入睡时间点是一个潜在的独立心血管风险因素。
信源:Shahram Nikbakhtian, et al. Accelerometer-derived sleep onset timing and cardiovascular disease incidence: a UK Biobank cohort study, European Heart Journal - Digital Health, 2021;, ztab088, https://doi.org/10.1093/ehjdh/ztab088.
09
Mol Cell:揭示感知需要睡眠的分子启动机制
睡眠对所有动物来说都是必不可少的,当我们疲惫不堪的时候,只要好好睡一觉,我们就能元气满满地开始新的一天啦。那么,我们究竟是如何知道自己需要睡觉的,晚上睡眠帮助机体修复的机制是什么?这些仍然是未解之谜。
一项来自以色列巴伊兰大学生命科学学院和多学科脑研究中心的研究发现斑马鱼的睡眠机制,并在小鼠上得到了证据支持,发现 DNA 损伤是睡眠的稳态驱动因素,而 Parp1 通路可以感知这种细胞压力并促进睡眠和修复活动。研究成果发表在2021年11月 Molecular Cell 杂志上。

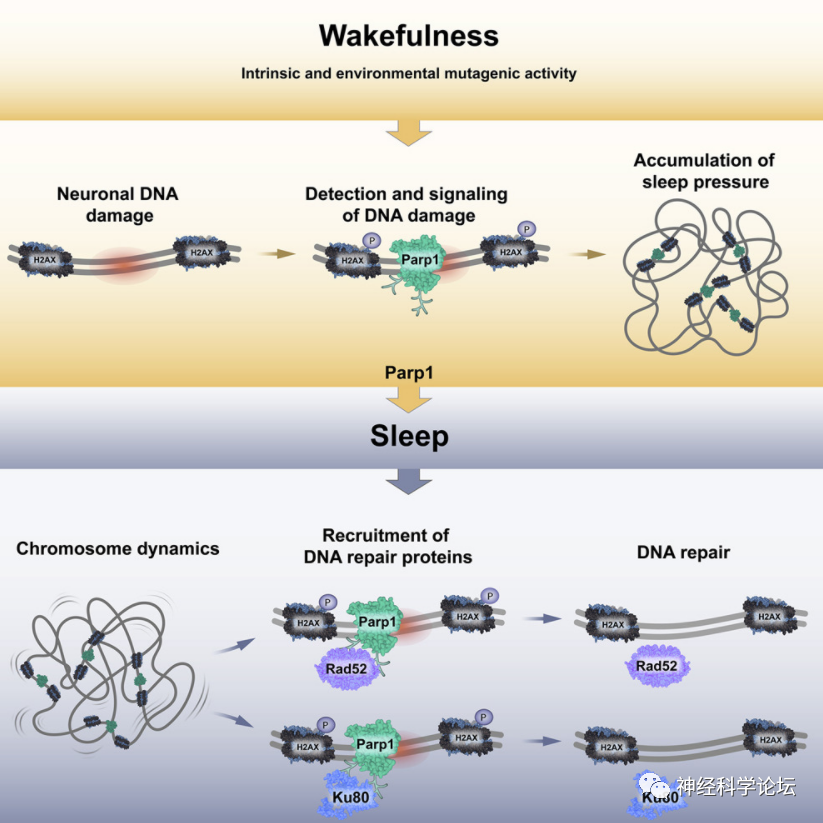
信源:Zada D,et al. Parp1 promotes sleep, which enhances DNA repair in neurons. Mol Cell. 2021 Nov 12:S1097-2765(21)00933-3. doi: 10.1016/j.molcel.2021.10.026.
本文内容转载来源以上网址及公众号。以上内容仅供学习使用,以上观点不代表本公众号,不作其它用途,如有侵权,请留言联系,作删除处理!
有任何疑问及建议,扫描以下公众号二维码添加交流:
